生命系統的形成離不開自組裝的作用,自然界中的氨基酸、多肽、蛋白質和DNA等天然分子通過協作自組裝發揮著重要的生物功能。借鑒這種自下而上的組裝過程,科研工作者在生命科學和材料工程領域構筑了豐富的功能結構材料。其中,自組裝形成的球形晶體聚合物不僅具有巨大的比表面積和獨特的晶體結構,其演化過程更是對神經退行性疾病(如阿爾茨海默癥)的發病與診斷提供了研究模型,近年來已成為生物傳感、藥物輸送、組織工程的研究熱點。因此,控制球晶形態并探索球晶生長機制是增強材料性能和實現疾病治療的關鍵環節。傳統球晶的制備方法通常依賴于對前驅體飽和溶液或聚合物熔體溫度的精確調控,增加了開發不同形貌球晶和探索其自組裝機理的難度。盡管在稀溶液中自組裝形成球晶的模型近期已有報道,但該方法仍需預先制備復雜的聚合物,并通過精確控制溫度和孵育時間來控制球晶的形貌。
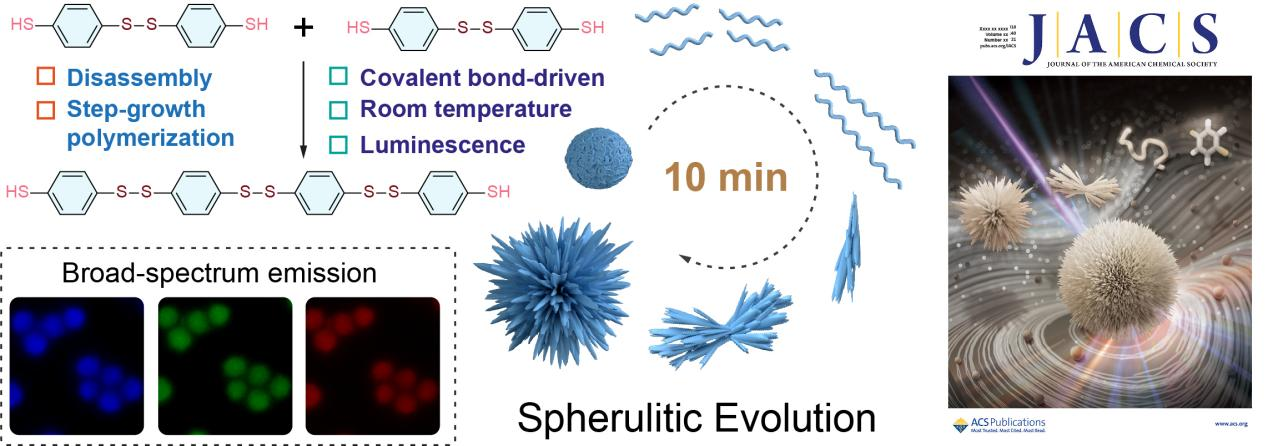
近日,四川大學周加境研究員與加州大學圣地亞哥分校Jesse V. Jokerst教授團隊合作,開發了一種在常溫下通過小分子均聚和自組裝形成的球形晶體聚合物(rPBDT),研究了其組裝機理并證明了其用于可示蹤藥物載體的潛力,該研究成果以題為“Self-Assembled Homopolymeric Spherulites from Small Molecules in Solution”發表于國際化學頂級期刊《Journal of the American Chemical Society》(川大A-),并入選封面論文。研究以小分子1,4-苯二硫醇(Benzene-1,4-dithiol,BDT)為原料,BDT分子的巰基首先在堿性緩沖溶液中形成雙硫鍵,進而逐步聚合形成聚合物鏈,苯環間的π-π堆積導致聚合物鏈組裝成超分子納米粒子(PBDT)。PBDT不僅尺寸均一(70.8 ± 8.7 nm),還可以通過種子生長法進一步生長至450 nm。將PBDT納米粒子置于良溶劑二甲基甲酰胺(DMF)中,苯環間的π-π堆積被破壞,導致PBDT分散并暴露出活性巰基,從而通過雙硫鍵進一步的逐步聚合形成分子量更大的聚合物鏈并最終結晶形成球晶(rPBDT)。該溶解和逐步聚合的過程可以在1 min內實現。通過監測rPBDT的生長過程,研究發現rPBDT鏈首先組裝成單個尖刺,然后多個尖刺從同一個中心生長形成束狀,最后大量尖刺從中心延伸發散,組裝形成準球形的rPBDT球晶。通過改變PBDT納米粒子的濃度,可制備具有不同尖刺數量的rPBDT球晶。此外,rPBDT球晶還具有優異的溶劑穩定性,在四氫呋喃(THF)中多次浸泡,形貌幾乎沒有改變。研究還發現,rPBDT具有在球晶領域鮮有報道的熒光特性,其原因可能是剛性雙硫鍵和超分子結構的存在導致了聚合物鏈上的苯環旋轉受阻,進而形成簇聚誘導發光(Clusterization-triggered emission,CTE)的現象。體外細胞毒性實驗證明rPBDT球晶具有優良的生物相容性,表明其作為可示蹤藥物載體的巨大潛力。圍繞rPBDT球晶自組裝機理的研究證明了共價鍵在球晶形成過程中的重要作用,這也是以往研究工作中容易忽視的一個方面。
該文通訊作者為我院周加境研究員以及加州大學圣地亞哥分校Jesse V. Jokerst教授,第一作者為四川大學輕工科學與工程學院科研助理宋欠濤。四川大學化學工程學院工程實驗教學中心黃艷萍實驗師對本工作提供了大力支持。該研究進一步推動了我院在小分子自組裝領域的發展,并為可示蹤藥物載體的研究提供了新思路。
該研究工作得到了中央高校基本科研業務費專項資金與皮革化學與工程教育部重點實驗室(四川大學)開放課題基金的資助。
文獻鏈接:https://pubs.acs.org/doi/abs/10.1021/jacs.3c08356